美國食品及藥物管理局(FDA)自2018年5月批出注射藥物Aimorig預防偏頭痛,9月底,再批准Galcanezumab預防成人偏頭痛。
偏頭痛(Migraine)是以嚴重頭痛反覆發作為特徵的神經系統疾病,常伴有其他症狀,包括惡心、嘔吐、對光和聲音敏感,患者的典型症狀更會有視力變化及看到閃光。據統計,3800多萬美國人患有偏頭痛,其中受偏頭痛影響的女性比男性多三倍。在約40%患有偏頭痛的患者中,只有13%患者接受治療。
致殘疾患
第二次國際偏頭痛研究(The Second International Burden of Migraine)結果表明,高達53%的研究受訪者表示因為副作用而停止了偏頭痛預防性治療。由於偏頭痛影響患者生活及工作,2012年,世界衛生組織將偏頭痛定性為致殘疾患的第七位,多年來,不少製藥公司亦不懈於研究預防及治療偏頭痛的藥物。
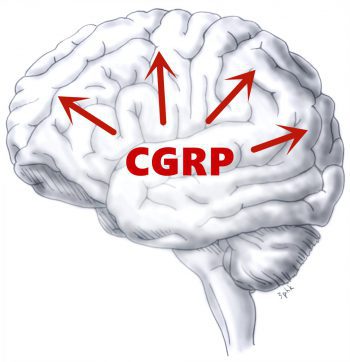
二十世紀時,大部分研究認為偏頭痛的主要機制在於血管擴張以及神經血管結構問題引起疼痛,而愈來愈多動物實驗和人體研究表明,皮質下腦區在偏頭痛具有相關作用。現時科學家認為皮質下結構和血管擴張以外的神經遞質才是偏頭痛的關鍵,亦發現偏頭痛發作時血液出現凝固狀態,可能與刺激了三叉神經及鈣素基因相關肽(Calcitonin Gene-related Peptid,CGRP)大量釋放有關。所以,CGRP成為了研究偏頭痛的重點。
CGRP
降鈣素基因相關肽(CGRP)是一個強力的血管舒張因子。神經學家發現CGRP可驅動偏頭痛的初期症狀,從急診就醫的偏頭痛患者頸靜脈中測到大量CGRP存在,證明CGRP於疼痛過程中釋放。由此致病機轉發現,如果抑制CGRP,即可預防或減少偏頭痛發作。
Galcanezumab是結合抑制降鈣素基因相關肽(CGRP)的活性單克隆抗體,該肽分子被認為在偏頭痛和叢集性頭痛(Cluster Headache)中起作用。作為一種每月一次的自我注射制劑,Galcanezumab旨在用於預防偏頭痛和叢集性頭痛。
FDA決定批准Galcanezumab使用於預防成年人偏頭痛是基於三項3期研究(EVOLVE-1、EVOLVE-2和REGAIN)均達到主要終點。與安慰劑相比,兩個研究劑量都在統計學上顯著減少每月偏頭痛的頭痛發作日數。
EVOLVE-1和EVOLVE-2在6個月的時間內進行,伴有偶發性偏頭痛的參與者隨機分為Galcanezumab 120mg、240mg或安慰劑。在EVOLVE-1中,使用120mg的參與者平均發病減少了4.7天,使用240mg組別則4.6天;而安慰劑則平均減少2.8天。在EVOLVE-2中,120mg組平均減少為4.3天,240mg組別的平均減少為4.2天,而安慰劑則平均減少2.3天。
REGIN對慢性偏頭痛患者的試驗在11個參與者中進行了為期三個月的研究。參與者平均每月偏頭痛天數顯著減少:120mg組為4.8天,240mg組為4.6天,而安慰劑組平均減少2.7天。
Galcanezumab處方資料列出的推薦劑量為240mg(兩次120mg注射)作為初始負荷劑量,然後每月120mg皮下注射。以注射器形式可以注射到腹部、大腿、上臂後部或臀部。
最常見的不良反應是注射部位反應。這些反應發生在18%接受Galcanezumab的臨床試驗患者中,而接受安慰劑的患者為13%。還發生了過敏反應,如皮疹、蕁麻疹和呼吸困難。3