改造沙門氏菌 「YB1」可望製成標靶藥
香港大學李嘉誠醫學院生物醫學學院的研究團隊最近成功將沙門氏菌改造成一種名為「YB1」的厭氧細菌,此細菌只能在癌腫瘤等缺氧環境中生長及繁殖,令癌腫瘤生長被有效抑制,又不會危害正常細胞。
沙門氏菌常見於未熟透的肉類、生雞蛋及蛋製食品,是引致食物中毒的病原體,一般會引起嘔吐、腹瀉及腹痛。香港大學醫學院生物醫學學院的研究團隊最近成功將沙門氏菌改造成一種名為「YB1」的厭氧細菌,可望為癌症病患者帶來新的治療希望。
厭氧細菌
香港大學醫學院生物醫學學院研究團隊透過最先進的基因工程重組技術,以及運用合成生物學的概念,成功將沙門氏菌改造成一種「專性」厭氧細菌,並命名為「YB1」。「YB1」不僅保存了沙門氏菌原有的毒性,而且只會在缺氧環境中(如人類體內的腫瘤)生存,更不會對正常含氧組織造成損傷。因此,以「YB1」作為標靶,能在不傷害身體其他正常組織的前提下選擇性地針對腫瘤,成為一種更安全地對抗癌症的臨床工具。研究團隊最近已透過香港大學技術轉移處成功為「YB1」厭氧細菌取得美國專利,同時亦正為這項技術向多個國家及地區申請專利,期望未來可將「YB1」製成針對腫瘤的標靶藥物。
利用肝癌和乳腺癌的小鼠模型,研究團隊初步證明了「YB1」是有效及安全的癌症治療方案。實驗結果顯示,「YB1」能在腫瘤內部繁殖並有效地抑制腫瘤轉移,相反在正常組織中則被迅速清除。在乳腺癌的小鼠模型中,「YB1」可令腫瘤的生長速度減緩約50%,而且能完全抑制腫瘤的肺轉移。在肝癌的小鼠模型中,「YB1」可充分抑制腫瘤的生長,和對照組相比,抑制程度高達九成。研究指除了肝癌及乳腺癌,「YB1」亦有抑制其他腫瘤生長的效果,例如神經母細胞瘤。
YB1導彈
目前,研究團隊正致力於開發這種新型細菌的其他用途。領導是次研究的香港大學醫學院生物醫學學院教授黃建東教授表示:「『YB1』具有選擇性地在腫瘤中生長的特性,它可以被視爲一種導彈,通過攜帶各種治療性蛋白質和藥物,將破壞性的彈頭運送至腫瘤組織中,消除腫瘤。」
為進一步提升療效,研究團隊利用「YB1」攜帶不同的藥物治療癌症。實驗顯示,在乳腺癌小鼠模型中,攜帶白喉毒素的「YB1」不但能百分百抑制腫瘤生長,而且可以令腫瘤縮小及促使腫瘤細胞死亡,腫瘤在26%的小鼠中完全消失,徹底治愈癌症。在治療後觀察的4個星期內,細菌治療組的小鼠全數生還,而實驗中對照組的小鼠則在第15天左右全部死亡。預計「YB1」可於數年後可進入臨床試驗階段。
利用細菌治腫瘤
癌症是最致命的疾病之一,目前的治療方法,如化療或放射治療並不能治愈大部分的癌症患者。由於腫瘤細胞迅速增加及腫瘤區域血液供應不足,導致腫瘤內往往出現缺氧的情況,而缺氧與腫瘤對治療出現抗藥性有密切的關係。缺氧可激發腫瘤細胞適應不良環境,防止腫瘤細胞死亡及促進腫瘤惡化,因此令治療對腫瘤細胞的殺傷效果大打折扣。
近年利用細菌治療腫瘤已經成爲癌症治療研究的一個新興領域。早在19世紀90年代,人類已發現感染厭氧細菌可消除部分或整個惡性腫瘤,然而,患者往往亦會因細菌嚴重感染而死亡。當時醫學界並不知道如何控制細菌的感染以提升治愈率。隨著基因工程技術和合成生物學的發展,這種情况已逐漸改變。現在研究人員可利用基因工程技術改造細菌,使其更適用於癌症治療。3
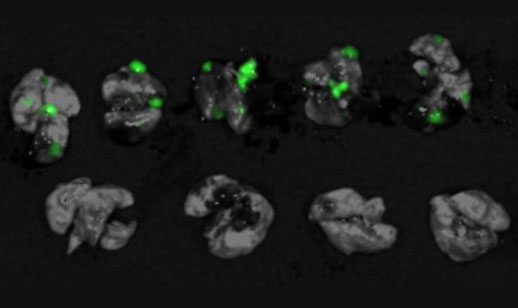
圖中顯示使用「YB1」治療乳腺癌肺轉移小鼠的情況,上方的綠色信號為對照組小鼠乳腺癌肺轉移的情況,而下方治療組小鼠以「YB1」治療後則沒有出現肺轉移。

港大研究團隊透過最先進的基因工程重組技術,以及運用合成生物學的概念,成功研發「YB1」厭氧細菌,並取得美國專利。