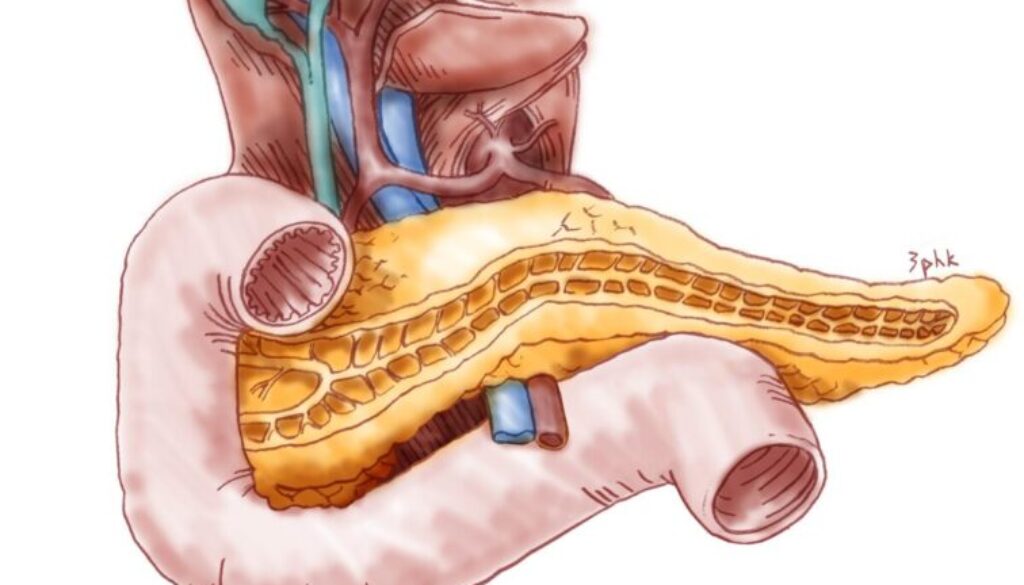
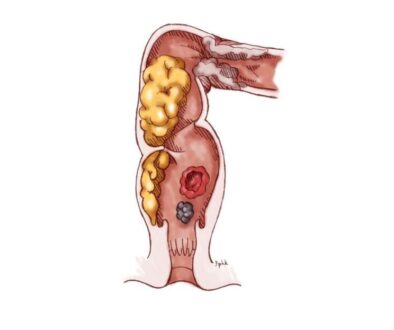
電場療法可居家治療胰臟癌
早於2020年,電場療法結合化療已被批准使用於膠質母細胞瘤治療,這款便攜設備最近被FDA批准用於治療局部晚期胰臟癌。
根據美國國家癌症研究所(National Cancer Institute)發布的資料,2025年美國新增約67,440例胰臟癌病例,並導致51,980人死亡。胰臟癌約佔所有新發癌症病例的3.3%,但由於其發現較晚,病情進展迅速且治療選擇有限,其死亡人數佔比卻異常高。
物理性治療
由於胰腺癌患者的診斷較困難,早期症狀與腸胃不適類似,常致發現時往往為中後期階段。胰臟癌可説是最難治療的癌症之一,患者長期以來一直渴望獲得更新的治療選擇。
美國食品及藥物管理局(FDA)批准一款用於治療局部晚期胰臟癌(Pancreatic Cancer)成年患者的創新設備。這是一款便攜式非侵入性設備,可將交變電場,又稱為腫瘤治療電場(Tumor Treating Fields,TTFields)輸送到腹部干擾癌細胞生長。TTFields是物理性抗癌治療,已用於治療膠質母細胞瘤(Glioblastoma,GBM),其原理是透過物理方式干擾癌細胞快速分裂的特性,同時最大限度地減少對健康組織的傷害。此次批准提供了一種全新的、非侵入性的治療方法,可以融入患者的日常生活,從而將癌症治療的覆蓋範圍擴展到傳統臨床環境之外。
FDA表示,希望將有前景的療法帶給真正需要的患者,這些器材旨在應對慢性疾病,改善病人的生活。該療法透過貼在患者皮膚上的絕緣貼片進行治療,這些貼片與電場發生器相連。設備的治療技術參數由製造商預設,患者或醫生均無法調整。患者需接受設備使用培訓,包括如何充電和更換設備電池、如何將設備連接到外部電源、如何將貼片貼在身體的適當位置,以及每周至少把換能器陣列更換兩次等等。該設備設計為可佩戴,使患者能夠在進行日常活動的同時接受持續治療。
總存活期稍長
FDA對其批准是基於一項在「研究性器械豁免」 (Investigational Device Exemption,IDE) 下進行的關鍵性臨床研究的數據。這項隨機對照研究對局部晚期胰腺癌成年患者進行了長達五年的追蹤。結果顯示,與單獨使用吉西他濱(Gemcitabine)合併白蛋白紫杉醇 (nab-Paclitaxe,GnP) 標準化療方案相比,在GnP方案中加入TTFields可使病患者總存活期延長約兩個月。研究中觀察到的最常見的器械相關風險是局部皮膚反應。
FDA授予這種TTFields為突破性醫療器材認定。突破性醫療器材認定旨在加快開發和審查能夠更有效地治療或診斷危及生命或造成不可逆轉的衰弱性疾病或病症的器械。3