口服藥治療輕中度新冠肺炎
新冠疫情擾攘多時,全球科學家都希望可攻克病毒,令人類生活回復正常,除了疫苗防預外,抗病毒藥物亦傳來好消息。
美國藥廠Merck與Ridgeback Biotherapeutics共同研發的抗新冠病毒藥物Molnupiravir試驗,發現可降低50%新冠患者的住院風險或死亡風險。Merck馬上向美國食品及藥物管理局(FDA)遞交上市申請,並承諾會在安全監管下進行全球範圍的應用。
阻斷病毒複製
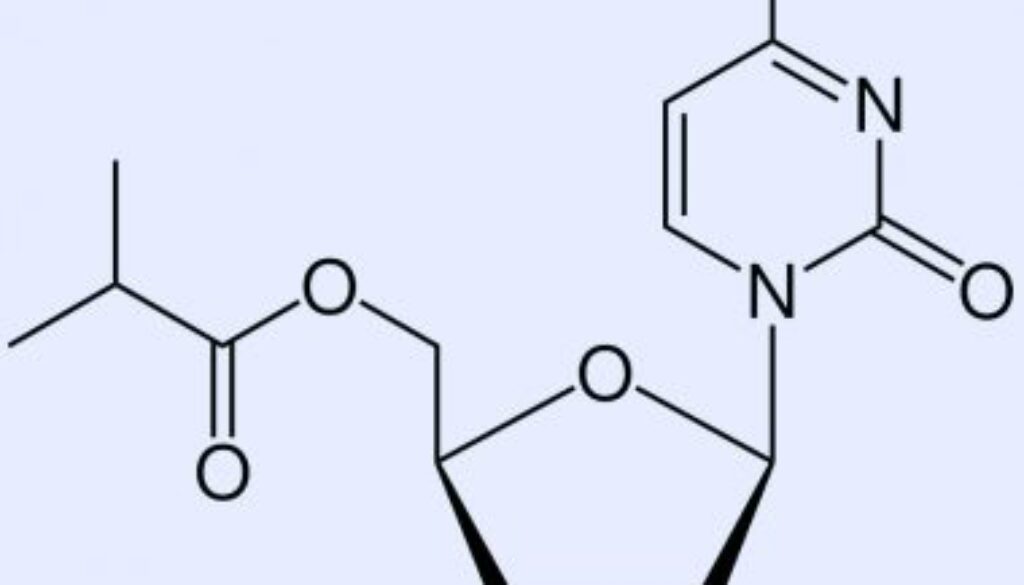
Molnupiravir是一種核苷類似物,能破壞依賴病毒RNA聚合酶的工作,這種酶對嚴重急性呼吸綜合症冠狀病毒2型(SARS-CoV-2)等RNA病毒的複製至關重要。與大多數針對病毒外刺狀蛋白的冠狀病毒疫苗不同,Molnupiravir是通過干擾病毒用於自我複製的聚合酶來消滅病毒,原理是通過將錯誤的基因片段引入病毒的基因密碼中,使病毒不能在人體內大量複製繁殖,從而中斷病毒的子代產生。
Merck公司傳染病研發部門副總裁Daria Hazuda指,運用Molnupiravir對未接種疫苗或疫苗免疫反應較差的人進行治療,是幫助結束新冠大流行一個重要的工具。該公司表示,截至目前的病毒測序顯示,Molnupiravir對冠狀病毒的所有變異毒株都有效,原因是Molnupiravir具有廣譜性的優點。現時疫苗和中和抗體一般都是針對病毒表面的S蛋白,而S蛋白相對容易突變,令中和抗體失效。因此預期Molnupiravir對新冠病毒的不同變異株,甚至其他種類的冠狀病毒都能發揮作用。
在一項第三期臨床試驗中,研究人員讓被診斷為新冠肺炎的患者,每天服用兩次Molnupiravir膠囊。在對775名患者分析後發現:於每天服用兩次Molnupiravir的患者中,有7.3%的人曾經因重症住院,而且在治療後29天內沒有人死亡。相比之下,安慰劑組患者的重症住院率高達14.1%,在安慰劑組中有8人在30天內死亡。鑑於研究結果正面,Merck提前結束該項試驗,向FDA申請緊急使用。
據Merck表示,試驗結果非常有效,不過,這些數據來自該公司的新聞稿,尚未經過同行評審。就安全性而言,臨床試驗中藥物組與安慰劑組不良反應出現的概率相當,證明藥物具有相當高的安全性,但在廣泛使用後,安全性還需要更多關注和研究。
早期用藥有效
Merck試驗結果表明,在患病早期服用Molnupiravir才能產生效果。輕中度非住院COVID-19患者條件為:18歲以上,PCR確診感染SARS-CoV-2,必須在症狀出現後五天內接受Molnupiravir治療。
目前,新冠肺炎患者的治療方案,包括使用Remdesivir和類固醇,這兩種藥物通常只在患者住院後使用。而Molnupiravir為口服藥,簡單易用,成本相對較低,在治療上有助於快速做到廣泛可及,但只有早期用藥療效才會明顯。此前一項研究發現,該藥對重症患者幾乎沒有幫助。
試驗數據顯示,Molnupiravir不會誘導人類細胞的基因變化,但為了安全起見,以及保護人類基因不受影響,參加該試驗的男性必須避免異性性行為或同意使用避孕措施。可能已懷孕的育齡女性亦必須使用避孕措施。Molnupiravir試驗的參與總人數不是特別多,在實際的大規模應用中,數字可能會有偏差,此外還需考慮疾病狀態、年齡、性別等。而且這是一種核苷酸類似物,仍需考慮潛在的長期毒性。
Merck預計到2021年底將生產1000萬個療程,預計2022年將生產更多劑量。早前,Merck與美國政府簽訂了採購協議,根據該協議,Merck將在緊急使用授權(EUA)或FDA批准後向美國政府供應約170萬個Molnupiravir療程。此外,Merck亦與世界其他國家政府簽訂了供應和採購協議,正在等待監管授權。該公司亦與成熟的仿製藥製造商就Molnupiravir達成非排他性自願許可協議,以加快Molnupiravir在百多個低收入及中等收入國家(LMIC)的供應。
不等同疫苗
新冠疫苗已經在很大程度上降低了新冠感染的危害,對降低重症和死亡風險尤其顯著。當然有效的抗病毒藥物亦是控制新冠疫情的一個關鍵措施。抗病毒藥物一般作為感染病毒後使用的治療藥物,無法替代疫苗作為預防病毒感染的效用。3